|
|
"ЖУРНАЛ РАДИОЭЛЕКТРОНИКИ" N 11, 2005 |
|
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЗРЕАГЕНТНО-МОДИФИЦИРОВАННОЙ ВОДЫ И ЕЁ БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ
Ю.В. Гуляев*, С.М. Еремин*, И.А. Марков*, Е.Г. Новоселова**,
В.В. Новиков**, Ю.А. Тен*, Е.Е. Фесенко**
*) Институт радиотехники и электроники РАН
**) Институт биофизики клетки РАН
Получена 08 ноября 2005 г.
Аннотация
Эмпирически установлено, что в сильных пространственно-неоднородных полях дистиллированная вода приобретает аномальные физико-химические свойства, в частности, зависимости ОВП от рН и дипольного момента от температуры, не укладывающиеся в рамки классических описаний. В данной работе предложена модель структурно-энергетической модификации воды, качественно объясняющая наблюдаемые свойства. Показано, что такая модифицированная вода приобретает биологическую активность: увеличивает в 3-4 раза синтез фактора некроза опухолей иммунно-компетентными клетками как in vivo, так и in vitro, приводит к ингибированию обратной транскриптазы вируса иммунодефицита человека, а также к ускорению спонтанного гидролиза белков в растворах.
Физико-химические свойства БМВ
К настоящему времени накоплен обширный объём достоверных, эмпирически установленных фактов, свидетельствующих о том, что вода, подвергнутая безреагентному (без привлечения химических реагентов) воздействию различными физическими полями, приобретает аномальные свойства, которые не находят объяснений в рамках общепринятой классической концепции, согласно которой все аномалии воды являются следствием привнесённых в неё примесей. Аномальные свойства безреагентно-модифицированной воды (БМВ) проявляются при сравнении её макрофизических и химических характеристик с соответствующими характеристиками её химического аналога – воды, не подвергнутой указанному воздействию. Одним из ярчайших свойств БМВ является их метастабильный характер, когда в условиях изоляции от внешних, включая химических, воздействий, физико-химические свойства БМВ с течением времени релаксируют к свойствам её химического аналога, что позволяет характеризовать БМВ как метаводу.
Ранее [1] сообщалось, что в сильных, пространственно-неоднородных электрических полях, дистиллированная вода, без привлечения химических реагентов, приобретает свойства, не согласующиеся с её химическим составом. Было показано, что для данной БМВ (дистиллированной воды, подвергнутой воздействию электрическими полями), при отсутствии в её составе щелочных элементов, показатель рН может достигать значений 9-11. При этом электропроводность БМВ в 8 – 30 раз превышает электропроводность её химического аналога. Был установлен также и метастабильный характер указанных свойств.
В последующем был выявлен ещё ряд физико-химических свойств БМВ, не укладывающихся в классическую концепцию. На Рис.1 представлена зависимость ориентационной поляризуемости БМВ от температуры. Там же для сравнения приведены зависимости для пиролизной воды (литературные данные), дистиллированной воды, подвергаемой воздействию электрическими полями и химического аналога БМВ.
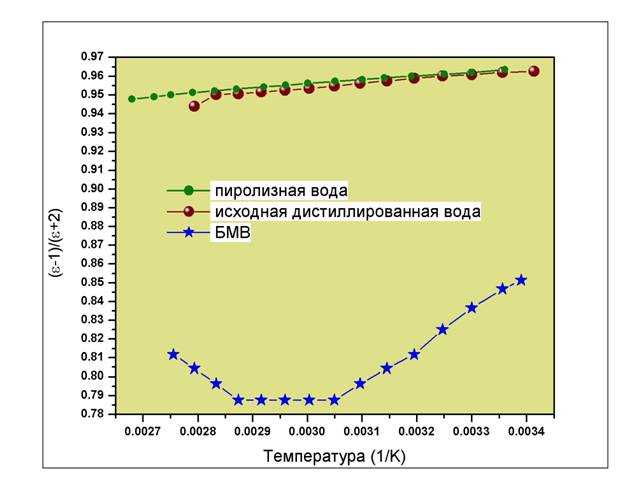
Рис.1. Зависимости ориентационной поляризуемости БМВ, пиролизной и бидистиллированной воды от температуры
Как
известно (теория Дебая), данная зависимость позволяет оценить ориентационную
молекулярную поляризацию и рассчитать величину дипольного электрического
момента молекул, входящих в состав тестируемых жидкостей. Сопоставление
приведённых зависимостей показывает, что величина дипольного момента молекул
БМВ в интервале температур 22 – 55![]() превышает соответствующее значение для
дистиллированной воды и химического аналога БМВ и составляет 5.23 D (для дистиллированной воды и
химического аналога БМВ дипольный момент равен 1.84 D).
превышает соответствующее значение для
дистиллированной воды и химического аналога БМВ и составляет 5.23 D (для дистиллированной воды и
химического аналога БМВ дипольный момент равен 1.84 D).
Обращает
на себя внимание существование на указанной зависимости для БМВ двух
температурных интервалов, в одном из которых (55 – 75![]() ) поляризуемость остаётся
неизменной, а в другом (75 – 90
) поляризуемость остаётся
неизменной, а в другом (75 – 90![]() ) происходит повышение поляризуемости с
увеличением температуры. Возможным объяснением указанных аномалий может служить
зависимость изменения молекулярной массы БМВ от температуры, когда с её
повышением масса уменьшается. В этом случае зависимость диэлектрической
проницаемости БМВ от температуры может быть обусловлена двумя конкурирующими
факторами:
) происходит повышение поляризуемости с
увеличением температуры. Возможным объяснением указанных аномалий может служить
зависимость изменения молекулярной массы БМВ от температуры, когда с её
повышением масса уменьшается. В этом случае зависимость диэлектрической
проницаемости БМВ от температуры может быть обусловлена двумя конкурирующими
факторами:
· температурным, когда согласно Дебаю диэлектрическая проницаемость уменьшается с ростом температуры и
· массовым, когда с ростом температуры уменьшается молекулярная масса полярной молекулы БМВ.
Преобладание одного из факторов над другим в определённых температурных интервалах может служить объяснением указанной аномалии зависимости поляризуемости БМВ от температуры.
На Рис.2 представлены положения ковариантных пар характеристик БМВ: рН – ОВП (окислительно-восстановительный потенциал), измеренных стандартными методами аналитической химии. Для сравнения приведены соответствующие положения пар для растворов Ca(OH)2 с различными значениями рН. ОВП измерялся в системе электродов Рt –ХСЭ (хлорсеребряный электрод).
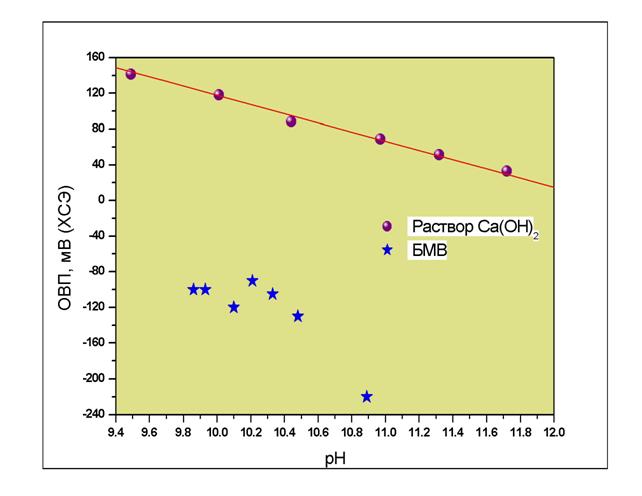
Рис.2. Зависимость ОВП от рН.
В рамках классических концепций, ковариантная пара значений рН – ОВП однозначно связана соотношением Нернста, согласно которому ОВП водных растворов неорганических веществ и соединений, измеренный в указанной системе электродов, не может иметь отрицательных значений. Существование отрицательных значений ОВП является, на наш взгляд, наиболее значимым подтверждением аномальности физико-химических свойств БМВ, ибо в этом случае исключается роль привнесённых в неё примесей в объяснении такой аномальности.
Подтверждением
метастабильного характера аномальных свойств БМВ служит зависимость ![]() ОВП (разницы между
измеренным значением ОВП для БМВ и значением ОВП раствора с тем же, что и для
БМВ показателем рН) от времени (Рис.3). Начальные значения составляли
соответственно:
ОВП (разницы между
измеренным значением ОВП для БМВ и значением ОВП раствора с тем же, что и для
БМВ показателем рН) от времени (Рис.3). Начальные значения составляли
соответственно:
для БМВ – рН = 10, ОВП = –21 мВ
и для раствора Ca(OH)2 – рН = 10, ОВП = +135 мВ.
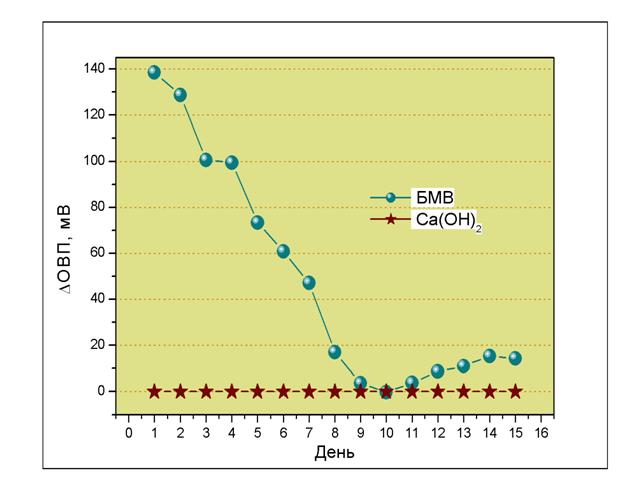
Рис.3.
Изменение «аномальности» БМВ (![]() ОВП) во времени.
ОВП) во времени.
Анализ
фактических данных по химическому составу БМВ, электропроводности, поляризуемости,
рН и ОВП позволяет предположить, что в процессе воздействия на дистиллированную
воду сильными, пространственно-неоднородными электрическими полями происходит дополнительная
диссоциация молекул воды и формирование протонофильных – (H2O)p и
гидроксофильных (H2O)n кластеров, которые образуют положительные H+(H2O)p и отрицательные
![]() (H2O)n кластерные ионы:
(H2O)n кластерные ионы:
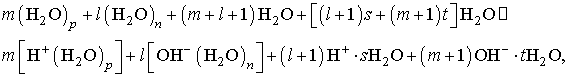 (1)
(1)
где p,n –
степени ассоциации аморфных молекул воды в протонофильных и гидроксофильных
кластерах, m и l
– концентрация протонофильных и гидроксофильных кластеров, ![]() – концентрация дополнительно
диссоциированных молекул воды, радикалы которых формируют кластерные ионы, s и t – степени
сольватации (гидратации) аморфными молекулами воды протона и гидроксила,
– концентрация дополнительно
диссоциированных молекул воды, радикалы которых формируют кластерные ионы, s и t – степени
сольватации (гидратации) аморфными молекулами воды протона и гидроксила, ![]() – количество аморфных
недиссоциированных молекул воды, формирующих сольватные (гидратные) оболочки
протонов и гидроксилов.
– количество аморфных
недиссоциированных молекул воды, формирующих сольватные (гидратные) оболочки
протонов и гидроксилов.
Предложенная модель позволяет дать качественное объяснение зарегистрированным аномальным свойствам БМВ. Так, если в (1) реализуется соотношение m > l, то при соблюдении электронейтральности, в БМВ будут выполняться условия основности (щелочности). Действительно, полагая, что кислотно-основные свойства определяются отношением концентраций сольватированных, не входящих в состав кластерных ионов протонов и гидроксилов из (1) в этом случае следует
![]() (2)
(2)
т.е. среда обладает щелочными свойствами при отсутствии в её составе щелочных элементов. Получает объяснение в рамках этой модели и повышенная электропроводность БМВ. Как известно, качественно электропроводность воды объясняется тремя типами механизмов переноса электрического заряда в электрическом поле – конвективный перенос заряда (закон Фарадея); эстафетный, когда сольватированный протон, покидая свою оболочку переносится полем к соседним аморфным молекулам воды с образованием новой гидратной оболочки и крокетный, когда пространственный перенос положительного заряда протона в электрическом поле происходит с участием ассоциированных молекулярных комплексов (кластеров). Наличие в БМВ повышенного, по сравнению с химическим аналогом, содержания амбиполярных радикалов воды и существование дополнительно сформированных кластеров приводят в этом случае к повышению электропроводности, обусловленной преимущественным, крокетным механизмом переноса заряда в электрическом поле. Поведение зависимости поляризуемости БМВ от температуры позволяет заключить, что для объяснения высоких значений дипольных молекулярных моментов, сформированные электрическим полем кластеры должны иметь линейную структуру и обладать большей, по сравнению с аморфными молекулами воды, стабильностью. Дипольный момент такого линейного кластера будет превосходить момент аморфной молекулы воды и момент «естественного» тетраэдрического кластера. Находит объяснение и метастабильный характер указанных свойств БМВ, когда с течением времени или под действием внешних факторов (температура, электрические поля, УФ облучение, вибрационное воздействие) линейные кластеры распадаются и свойства БМВ релаксируют к свойствам её химического аналога.
В заключение следует указать, что возможность формирования протонофильного кластера (H2O)6 была подтверждена экспериментально на основании результатов по ИК спектрометрии растворов HCl и HBr [2].
Биологические свойства БМВ
Особо интересны биологические свойства БМВ. Вода с этими характеристиками существенно влияет на физико-химические свойства и биологическую активность протеинов. Нами обнаружено методами флуоресцентной спектроскопии, что БМВ изменяет интенсивность собственной флуоресценции белковых молекул, а также влияет на процессы связывания протеинов с флуоресцентными зондами [3]. Эти эффекты могут быть обусловлены изменением в БМВ, по сравнению с исходным дистиллятом, микроокружения белковых молекул. Не исключено, что изменение микроокружения может повлиять на конформацию белка, что также отразится на спектрах флуоресценции. Нами также получены данные о существенном увеличении флуоресценции БМВ по сравнению с исходным контролем при возбуждении в ультрафиолетовой области [3]. Неясно, чем обусловлен данный результат. Заманчиво предположить, что наблюдаемые нами эффекты изменения показателей флуоресценции белков, могут быть обусловлены наличием в БМВ водных или водно-солевых структур (возможно типа клатратов).
Мы показали, что нахождение протеинов в БМВ при комнатной температуре в течение нескольких часов вызывает существенное (в десятки раз) ускорение процессов гидролиза белков и пептидов [4]. Пример такого ускорения приведен на рисунке 4. Важно отметить, что фрагменты гидролиза протеинов, отличаются по времени выхода с колонки при высокоэффективной жидкостной хроматографии (HPLC) от исходных молекул. Нахождение протеинов в БМВ в течение суток приводит к практически полному гидролизу исходных протеинов на пептидные фрагменты.
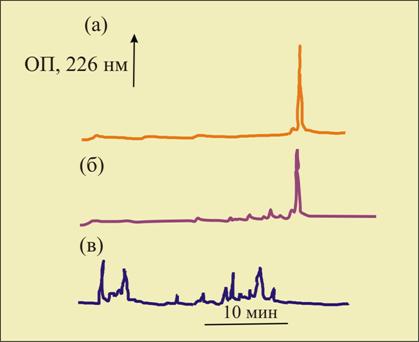
Рис. 4. Профиль элюции при HPLC: а – пептид (Б-цепь инсулина быка) в дистиллированной воде (контроль); б – пептид в БМВ (экспозиция 4 часа); пептид в БМВ (экспозиция 24 часа).
Мы обнаружили, что экспозиция протеинов в БМВ приводит к существенному изменению их функциональной активности [5]. Данный результат справедлив в отношении рекомбинантной обратной транскриптазы вируса иммунодефицита человека типа HIV-1. Пребывание этой ревертазы в БМВ приводит к существенному снижению ее РНК-зависимой ДНК-полимеразной активности. По-видимому, подобный эффект может иметь место и в случае других ключевых ферментов репродукции.
Особый интерес представляют данные по исследованию биологической активности БМВ на клеточном уровне и на уровне живого организма [6]. Нами показано, что добавка БМВ к макрофагам мыши in vitro в 3-4 раза повышает продукцию фактора некроза опухолей. Столь же значительная стимуляция фактора некроза опухолей отмечается и на уровне целого организма при пероральном потреблении БМВ. В этих условиях также в 1,5 раза возрастает активность естественных киллерных клеток селезенки. Стимуляция противоопухолевого иммунитета при пероральном потреблении БМВ приводит к подавлению роста экспериментальных опухолей (Рис. 5). Данные опыты были нами проведены на мышах-опухоленосителях с солидной формой АКЭ (асцитная карцинома Эрлиха). В этой связи важно отметить, что данная форма опухолей приводит к 100% гибели животных в контрольных случаях. В нашем случае, при пероральном использовании БМВ, мы не только отметили эффект торможения развития опухолей (защитный эффект), но и зарегистрировали отсроченный положительных результат, показавший полное излечивание приблизительно 30% животных (лечебный эффект). Опыты с БМВ в комбинации с цитостатиками показали, что БМВ хорошо сочетается с этими препаратами - эффекты БМВ и цитостатиков взаимно усиливаются.
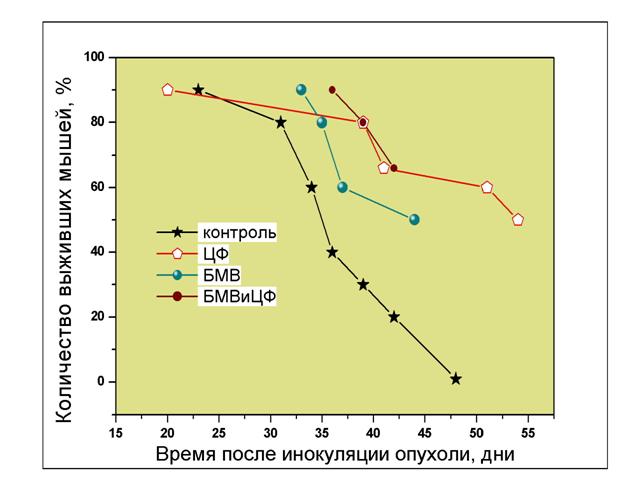
Рис. 5. Кривые гибели мышей с экспериментальными солидными опухолями: 1 – контроль; 2 – циклофосфан (ЦФ); 3 – БМВ; 4 – БМВ+ЦФ.
Важно отметить, что результаты, полученные в опытах с БМВ на биологических объектах, имеют сходство с данными, полученными нами ранее при анализе биологической активности слабых магнитных и электромагнитных полей [7,8]. В этих случаях мы также обнаружили выраженные эффекты на структурно-функциональные свойства белковых и пептидных молекул и выраженный противоопухолевый эффект. В этой связи следует особо отметить то, что совокупность всех полученных нами данных скорее свидетельствует в пользу предположения о ведущей роли в биологической активности БМВ не химических добавок (примесей), а, именно, «аномальных» физико-химических свойств БМВ, приобретенных в результате обработки воды физическими факторами.
Предварительные эксперименты показали, что указанный биологически активный фактор в БМВ подвергается выделению методом жидкостной хроматографии. Это позволяет получить фракцию, значительно более активную по сравнению с исходной БМВ в плане терапии экспериментальных опухолей у мышей.
Полученные нами результаты, указывающие на значительную биологическую активность БМВ, позволяют прогнозировать возможность его применения в медицине в качестве иммуномодулятора (для коррекции иммунного статуса), в терапии злокачественных новообразований, в терапии вирусных заболеваний и, возможно, в терапии заболеваний, вызываемых определенным типом белка (болезнь Альцгеймера).
Литература
- Ю.В. Гуляев, С.М. Еремин, И.А. Марков. Модификация структурно-энергетического состояния воды в электрическом поле // Радиотехника, №11, 1997, с.29-30.
- J. Kim, U.W. Schmitt, J.A. Gruenzmacher, G.A. Voth, N.E. Scherer. The vivration spectrum of the hydrated proton: Comparison of experiment, simulation, and normal mode analysis // J. of Chem. Phys., V.116, N2, 2002, pp.737-746.
- В.В. Кувичкин, В.В. Новиков, Ф.К. Алюшев, С.М. Еремин, И.А. Марков, Ю.А. Тен. Действие бидистиллированной модифицированной воды на конформационное состояние бычьего сывороточного альбумина // Биофизика.2001. Т.46, B.1. C.43-45.
- В.В. Новиков, А.С. Лисицын, Е.Е. Фесенко, Ф.К. Алюшев, С.М. Еремин, И.А. Марков, Ю.А. Тен. Гидролиз Б - цепи инсулина быка в бидистиллированной модифицированной воде // Биофизика.2001. Т.46, B.2. C.242-244.
- Ю.П. Швецов, В.В. Новиков, Е.Е. Фесенко, Ф.К. Алюшев, С.М. Еремин, И.А. Марков, Ю.А. Тен. Снижение РНК-зависимой ДНК-полимеразной активности рекомбинантной обратной транскриптазы вируса иммунодефицита человека в бидистиллированной модифицированной воде // Биофизика.2001. Т.46, B.2. C.379-380.
- Е.Е. Фесенко, Е.Г. Новоселова, В.Б. Огай, Т.А. Агафонова, О.В. Глушкова, О.А. Синотова, Ф.К. Алюшев, С.М. Еремин, И.А. Марков, Ю.А. Тен. Иммуномодулирующие свойства бидистиллированной модифицированной воды // Биофизика.2001. Т.46, B.2. C.353-358.
- В.В. Новиков, Е.Е. Фесенко. Гидролиз ряда пептидов и белков в слабых комбинированных постоянном и низкочастотном переменном магнитных полях // Биофизика.2001. Т.46, B.2. C.235-241.
- Е.Г. Новоселова, В.Б. Огай, О.В. Сорокина, В.В. Новиков, Е.Е. Фесенко. Влияние электромагнитных волн сантиметрового диапазона и комбинированного магнитного поля на продукцию фактора некроза опухолей в клетках мышей с экспериментальными опухолями // Биофизика.2001. Т.46, B.1. C.131-135.
|
|
|

