УДК 615.47:615.012.6
КОЛИЧЕСТВЕННЫЕ ПРИЗНАКИ РАННЕГО ПАРКИНСОНИЗМА
В ЭЛЕКТРОФИЗИОЛОГИЧЕСКИХ СИГНАЛАХ
О. С. Сушкова 1, Ю. В. Обухов 1, И. А. Малюта 2
1 Институт радиотехники и электроники РАН,
2 Московский физико-технический институт (государственный университет)
Статья получена 27 августа 2015 г.
Аннотация. Предложена модель электрофизиологических количественных признаков болезни Паркинсона на 1-й стадии качественной шкалы Хен-Яра, заключающаяся в оценках межполушарной асимметрии, дезорганизации электрической активности коры головного мозга, контралатеральной связанности электроэнцефалограмм, электромиограмм и тремора.
Ключевые слова: болезнь Паркинсона, механический тремор, электроэнцефалограмма, электромиограмма, акселерометр, частотная синхронизация, вейвлет-спектрограмма, огибающая электромиограммы.
Abstract. A model of electrophysiological quantitative signs of Parkinson's disease in the 1st stage of the Hoehn and Yahr scale is described. This model lies in an estimation of the hemispheric asymmetry, disorganization of the electrical activity of the cerebral cortex, and contralateral connectivity of electroencephalogram, electromyogram, and tremor.
Key words: Parkinson's disease, mechanical tremor, electroencephalogram, electromyogram, accelerometer, frequency synchronization, wavelet spectrogram, shape of the EMG.
Введение
Ранняя диагностика болезни Паркинсона (БП) до сих пор является не решенной задачей [1, 2]. Наиболее информативным методом считается позитрон-эмиссионная томография. Однако это очень дорогой метод, и он не может широко использоваться во врачебной практике для диагностики доклинической и начальной стадии. В этой связи возникает необходимость разработки новых систем диагностики БП и групп риска. Одним из подходов к решению задач диагностики раннего паркинсонизма являются электрофизиологические и механические исследования - электроэнцефалография (ЭЭГ), электромиография (ЭМГ), стабилография и акселерометрия. Электроэнцефалографические исследования, также как и исследования электромиографии мышц и механического тремора проводятся на более дешевом оборудовании по сравнению с установками нейровизуализации и поэтому могут широко применяться для скрининга населения с целью диагностики ранних стадий и выделения групп риска на доклинической стадии БП.
В работах [3-5] предложен и исследован новый метод диагностики БП, основанный на анализе частотно-временных свойств сигналов ЭЭГ, а в работе [6] – совместно измеренных сигналов ЭЭГ, ЭМГ и тремора конечностей. Были получены основные признаки БП на ранней стадии: межполушарная асимметрия частотно-временных характеристик ЭЭГ особенно в центральных отведениях (С3, С4); возникновение ритма в частотном диапазоне 4 - 6 Гц и его связанность с ритмами электромиографической активности и механического тремора конечностей в этом диапазоне; дезорганизация доминирующего ритма ЭЭГ, соответствующая общим представлениям о дезорганизации различных систем при БП.
В настоящей работе введена количественная мера в пространстве этих электрофизиологических признаков БП на 1-й стадии – эвклидово расстояние, и описаны результаты количественного сравнения этой меры для групп пациентов и контроля.
Модель количественных признаков 1-й стадии болезни Паркинсона
Рассмотрим следующую модель количественных оценок этих электрофизиологических признаков Pi в виде:
![]()
![]()
Здесь i ![]() {1, 2, 3, 4, 5} – номер признака, j,
j* - симметричные пары отведений ЭЭГ.
{1, 2, 3, 4, 5} – номер признака, j,
j* - симметричные пары отведений ЭЭГ.
Электрофизиологические признаки:
· max(T(L)/T(R),T(R)/T(L)) – отношение большей амплитуды тремора в «больной» руке к меньшей амплитуде в «здоровой»;
· Aθ/Aα(j) и Aθ/Aα(j*) – отношение амплитуд тета (4-6 Гц) и альфа (8-12 Гц) пиков частотных гистограмм экстремумов вейвлет спектрограмм в симметричных отведениях для выявления межполушарной асимметрии частотно-временных характеристик ЭЭГ;
· r(j)/r(j*) и σ(j*)/σ(j) – отношения коэффициентов корреляции динамических гистограмм доминирующего ритма (более 6 Гц) в контралатеральной «больной» руке отведения j или j* к симметричному отведению и отношение среднеквадратичных отклонений распределения.
В пространстве признаков Pi можно сформировать эвклидово расстояние Ri(j,j*) от испытуемого до абстрактного идеального объекта:
Ri(j,j*) = (∑i (Pi(j,j*) - Pi(идеал))2)1/2, (2)
где
Pi(идеал) = {1, 0, 0, 1, 1}. (3)
Значения признаков Pi(идеал) означают отсутствие тета ритма и симметрию остальных признаков. Выбор точки отсчета Pi(идеал) в эвклидовом признаковом пространстве Рi не является принципиальным для оценки расстояния между больным объектом и контрольным.
Больные и методы исследования
Были обследованы 31 пациент с БП дрожательно-ригидной формы на 1-й стадии по шкале Хен-Яра и 18 человек из контрольной группы испытуемых. Отбор пациентов осуществлялся на базе научного центра неврологии РАН, где ранняя стадия болезни Паркинсона у исследуемой группы пациентов была подтверждена клинически. Возраст группы пациентов: от 38 до 71 года, средний возраст – 58 лет. Возраст контрольной группы испытуемых: от 22 до 80 лет, средний возраст – 51 год. Одновременно регистрировались ЭЭГ, ЭМГ и механический тремор при помощи акселерометров. Для исследований ЭЭГ и ЭМГ использовался 41-канальный многофункциональный комплекс для проведения нейрофизиологических исследований “Нейрон-спектр-5” фирмы “Нейрософт”. При записи ЭЭГ и ЭМГ были включены фильтр верхних частот с частотой отсечки 0.5 Гц, а также режекторный фильтр 50 Гц. Использовалась частота дискретизации сигналов 500 Гц для записей ЭЭГ и ЭМГ, и 1378 Гц – для записей тремора.
Запись ЭЭГ осуществлялась по стандартной схеме 10х20 (рис. 1). Названия отведений ЭЭГ (индексы j, j* в уравнениях (1-2)) соответствуют схеме 10х20: Fp1 и Fp2, F7 и F8, F3 и F4, T3 и T4, C3 и C4, P3 и P4, T5 и T6, O1 и O2.
Рис. 1. Расположения электродов ЭЭГ по схеме 10х20.
Полученные данные обрабатывались с помощью программ, разработанных авторами. В частности, осуществлялась следующая предварительная обработка сигналов ЭЭГ:
1. Были использованы режекторные фильтры 50, 100, 150, 200 Гц для удаления сетевой наводки.
2. Сигнал ЭЭГ был отфильтрован фильтром Баттерворта. При этом применялась двухэтапная фильтрация – в прямом, а затем в обратном направлении сигнала, для устранения фазовых искажений сигнала при фильтрации. На каждом этапе применялся фильтр Баттерворта четвёртого порядка с полосой пропускания от 2 до 240 Гц.
3.
Была осуществлена
децимация сигнала, коэффициент децимации 4.
Распределение логарифмических значений R
Рассмотрим распределение логарифмических значений R от некой точки отсчета по всем парам отведений ЭЭГ в пространстве признаков для 31 пациента на первой стадии БП и 18 испытуемых из контрольной группы. Выбор точки отсчета не влияет на различия значений R между пациентами и контрольной группы испытуемых.
Логарифмические значения R для пары отведений С3-С4 для пациентов и контрольной группы испытуемых с учетом тремора представлены на рисунке 2, из которого видно, что группы пациентов (синие ромбики) и контроля (красные треугольники) достаточно хорошо разграничиваются между собой. Логарифмические значения пациентов в основном находятся выше 0, а контроль, в основном, – ниже 0.
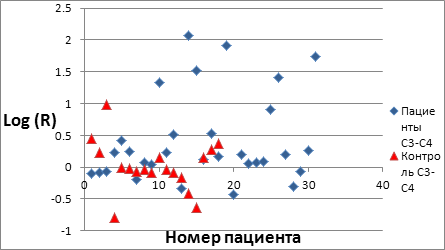
Рис. 2. Логарифмические значения R для пары отведений С3-С4 для пациентов
и контрольной группы испытуемых с учетом тремора.
Логарифмические значения R для пары отведений С3-С4 для пациентов и контрольной группы испытуемых без учета тремора представлены на рисунке 3, из которого видно, что группы пациентов (синие ромбики) и контроля (красные треугольники) также различаются. Однако, по сравнению с записями, где были учтены значения, полученные с акселерометра (рис. 2), здесь различие этих групп становится хуже (рис. 3) – большее число пациентов попадают в область, где находится группа контрольных испытуемых, то есть в область ниже 0.
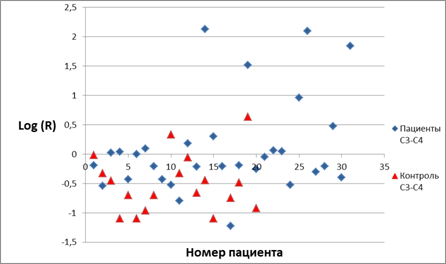
Рис. 3. Логарифмические значения R для отведений С3-С4 для пациентов
и контрольной группы испытуемых без учета тремора.
По полученным логарифмическим значениям R для групп пациентов и контроля как для записей с учетом тремора, так и без учета тремора были посчитаны средние арифметические значения и средние отклонения.
Распределение средних арифмитических значений и средних отклонений логарифмических значений R для пациентов и контрольной группы испытуемых без учета тремора представлено на рисунке 4. Для каждой пары отведений вычисляются средние арифметические значения логарифмических значений R и их средние отклонения.
Из этого распределения видно, что группы пациентов и контроля различаются, но не во всех отведениях достаточно хорошо. Самое лучшее же отличие между этими двумя группами наблюдается в паре отведений C3-C4, которые находятся в моторной зоне коры головного мозга.
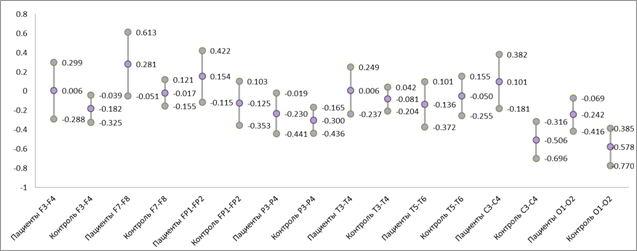
Рис. 4. Распределение средних арифметических
значений логарифмических
значений R и их средних отклонений
для всех пар
отведений для пациентов и контрольной группы испытуемых без учета тремора.
Однако, если учесть в этом распределении значения тремора, полученные при помощи акселерометра, то различия средних арифметических значений и средних отклонений логарифмических значений R по всем парам отведений между группами пациентов и контроля становятся более явными, что показано на рисунке 5.
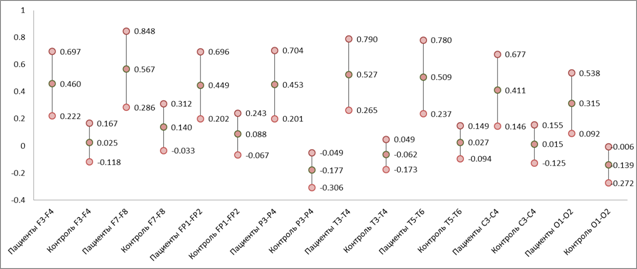
Рис. 5. Распределение средних арифметических
значений логарифмических
значения R и их средних отклонений
для всех пар
отведений для пациентов и контрольной группы испытуемых с учетом тремора.
Выводы
Проведены совместные электроэнцефалографические, электромиографические и акселерометрические исследования 31 нелеченого пациента на начальной стадии болезни Паркинсона дрожательной и дрожательно-ригидной форм и 18 волонтеров контрольной группы испытуемых.
Предложена модель электрофизиологических количественных признаков болезни Паркинсона на 1-й стадии качественной шкалы Хен-Яра, заключающаяся в оценках межполушарной асимметрии, дезорганизации электрической активности коры головного мозга, контралатеральной связанности электроэнцефалограмм, электромиограмм и тремора.
Показано распределение средних арифмитических значений и средних отклонений логарифмических значений R по всем парам отведений для пациентов и контрольной группы испытуемых без учета тремора. Из этого распределения видно, что группы пациентов и контроля различаются, но не во всех отведениях достаточно хорошо. Самое лучшее же отличие между пациентами и контролем наблюдается в паре отведений C3-C4, которые находятся в моторной зоне коры головного мозга, – что говорит о том, что именно эту пару отведений можно выбирать для дальнейшего более детального анализа и для постановки диагноза.
Показано, что в этом распределении при учете значений тремора, полученных при помощи акселерометра, различие средних арифметических значений и средних отклонений логарифмических значений R по всем парам отведений между группами пациентов и контроля становится очевидным.
Работа поддержана РФФИ, проект № 15-07-07846.
Литература
1. Угрюмов М.В. Новые представления о патогенезе, диагностике и лечении нейродегенеративных заболеваний // Вестник Российской Академии медицинских наук.-2010, № 8, C. 8-19
2. K. Brockmann, D. Berg. Diagnosis of Parkinson's Disease. Parkinson Disease and Other Movement Disorders (eds. e. Wolters. C. Baumann). - Int. Ass. of Parkinsonism and Related Disorders, VU University Press, 2014, P. 229-242
3. Обухов Ю.В., Королев М.С., Габова А.В., Кузнецова Г.Д., Угрюмов М. В. Способ ранней электроэнцефалографической диагностики болезни Паркинсона – Патент РФ № 2484766 от 20.06.2013
4. Обухов Ю.В., Габова А.В., Залялова З.А., Иллариошкин С.Н., Карабанов А.В., Кершнер И.А., Королев М.С., Кузнецова Г.Д., Морозов А.А., Нигматуллина Р.Р., Обухов К.Ю., Сушкова О.С. «Электрофизиологические подходы к диагностике болезни Паркинсона в ранней стадии» // Нейродегенеративные заболевания: от генома до целостного организма / под. ред. М.В. Угрюмова – Издательство "Научный мир", 2014, T. 1, C. 177-193.
5. Сушкова О.С., Габова А.В., Карабанов А.В., Кершнер И.А., Обухов К.Ю., Обухов Ю.В. «Метод частотно-временного анализа совместных измерений ЭЭГ, ЭМГ и механического тремора при болезни Паркинсона» //Нелинейный мир, № 2, т. 13, 2015, С. 49-51
6. О.С. Сушкова, М.С. Королев, А.В. Габова, С. Н. Иллариошкин, А. В. Карабанов, К.Ю. Обухов, Ю.В. Обухов. Совместный анализ сигналов электроэнцефалограмм, электромиограмм и механического тремора при болезни Паркинсона в ранней стадии. // Журнал Радиоэлектроники [электронный журнал]. 2014. N5. URL: http://jre.cplire.ru/jre/may14/12/text.html